| Valence -
Formule chimique des molécules et des radicaux |
INTRODUCTION | OBSERVATION | DEFINITION | VALENCE DES
ATOMES | VALENCE DES
RADICAUX
| RADICAL
ET MOLECULE
| EXERCICES 1 | EXERCICES 2 | MOTS
CROISES
 Introduction Introduction
 |
On connaît la formule de l'eau: H2O.
Pourquoi pas HO, HO2,
H3O, ... ? Le modèle ci-contre représente une
molécule d'eau; il a été obtenu, comme tout modèle,
à partir d'observations indirectes et d'hypothèses
vérifiées. Ce modèle ne correspond pas à la
réalité, mais il en constitue une représentation
suffisamment valable pour rendre compte des phénomènes
observés par les scientifiques.
Comment
s'associent les atomes entre eux pour former des ensembles
d'atomes appelés molécules?
|
INTRODUCTION | OBSERVATION | DEFINITION | VALENCE DES
ATOMES | VALENCE DES
RADICAUX
| RADICAL
ET MOLECULE
| EXERCICES 1 | EXERCICES 2 | MOTS
CROISES
 Observation de quelques modèles de molécules Observation de quelques modèles de molécules
| modèle d'une molécule de chlorure
d'hydrogène |
modèle d'une molécule d'eau |
modèle d'une molécule de gaz
ammoniac |
modèle d'une molécule de gaz
méthane |
 |
 |
 |
 |
formule chimique:
HCl |
formule chimique:
H2O |
formule chimique:
NH3 |
formule chimique:
CH4 |
points communs entre ces 4 molécules:
- la présence
de l'atome d'hydrogène H
- le nombre de
sortes d'atomes est 2 (composés binaires)
|
différences entre ces 4 molécules:
- l'atome
attaché à l'atome d'hydrogène H est différent
- le nombre
total d'atomes est différent
|
| 1 atome d'hydrogène H est
attaché a 1 atome de chlore Cl |
2 atomes d'hydrogène H sont
attachés à 1 atome d'oxygène O |
3 atomes d'hydrogène H sont
attachés à 1 atome d'azote N |
4 atomes d'hydrogène H sont
attachés à 1 atome de carbone C |
| 1 atome de chlore Cl est capable de s'accrocher
à 1 atome d'hydrogène H |
1 atome d'oxygène O est capable de s'accrocher
à 2 atomes d'hydrogène H |
1 atome d'azote N est capable de s'accrocher
à 3 atomes d'hydrogène H |
1 atome de carbone C est capable de s'accrocher
à 4 atomes d'hydrogène H |
| on dit que le chlore Cl a la valence I |
on dit que l'oxygène O a la valence II |
on dit que l'azote N a la valence III |
on dit que le carbone C a la valence IV |
INTRODUCTION | OBSERVATION | DEFINITION | VALENCE DES
ATOMES | VALENCE DES
RADICAUX
| RADICAL
ET MOLECULE
| EXERCICES 1 | EXERCICES 2 | MOTS
CROISES
 Définition de la valence Définition de la valence
| La valence d'un atome serait donc le
nombre d'atomes d'hydrogène que cet atome est capable de
fixer lors d'une réaction chimique; mais des molécules
ne contiennent pas l'atome d'hydrogène, comme dans le
cas du dioxyde de silicium (silice) SiO2
dont un modèle de la molécule est représenté
ci-contre (en rouge: l'atome d'oxygène O, en noir: l'atome de silicium Si) |
 |
| Cependant, nous savons que
l'oxygène a la valence II (voir tableau
précédent, deuxième colonne); dans la
molécule SiO2, 2 atomes d'oxygène sont
attachés à l'unique atome de silicium, donc celui-ci a
la valence IV. L'atome d'oxygène est capable de
remplacer 2 atomes d'hydrogène, le silicium a la même
valence que le carbone (voir tableau
précédent, quatrième colonne). |
INTRODUCTION | OBSERVATION | DEFINITION | VALENCE DES
ATOMES | VALENCE DES
RADICAUX
| RADICAL
ET MOLECULE
| EXERCICES 1 | EXERCICES 2 | MOTS
CROISES
 La valence des atomes: utilisation du tableau
périodique La valence des atomes: utilisation du tableau
périodique
Dans le cas des familles a (tableau plié), c'est facile:
famille
 |
Ia |
IIa |
IIIa |
IVa |
Va |
VIa |
VIIa |
O |
quelques atomes
 |
H, Na, K |
Be, Mg, Ca |
B, Al |
C, Si, Pb |
N, P |
O, S |
F, Cl, I |
He, Ne, Ar |
valence
 |
I |
II |
III |
IV |
III (8 - 5) |
II (8 - 6) |
I (8 - 7) |
0 (8 - 8) |
Les
atomes de la famille O (ou VIIIa) ne s'associent pas entre eux
ni avec d'autres atomes pour former des molécules: ce sont
des corps purs élémentaires puisque leur molécule n'existe
pas.
Malheureusement
des atomes des familles Va et VIa ne conservent pas toujours
la même valence (cas du plomb Pb: valence II ou valence IV)
ou se comportent comme s'ils possédaient une autre valence
que celle trouvée dans le tableau périodique (l'explication
de ces caractéristiques n'entre pas dans le cadre de cette
leçon).
Dans
le cas des familles b, c'est impossible (il y a trop
d'exeptions): il faut donc retenir la valence des atomes
principaux:
| nom de l'atome |
symbole |
valence(s) |
| argent |
Ag |
I |
| cuivre |
Cu |
I ou II |
| fer |
Fe |
II ou III |
| mercure |
Hg |
I ou II |
| or |
Au |
I |
| plomb |
Pb |
II ou IV |
| zinc |
Zn |
II |
INTRODUCTION | OBSERVATION | DEFINITION | VALENCE DES
ATOMES | VALENCE DES
RADICAUX
| RADICAL
ET MOLECULE
| EXERCICES 1 | EXERCICES 2 | MOTS
CROISES
 La valence des
groupements d'atomes ou radicaux La valence des
groupements d'atomes ou radicaux
Exemples de radicaux
| formule de composés |
formule du
radical |
nom du radical |
valence du
radical |
| NaOH, Ca(OH)2,
Al(OH)3 |
OH |
hydroxyle (ou hydroxyde) |
I |
| NH4Cl, (NH4)2O,
NH4OH |
NH4 |
ammonium |
I |
| HCN, NaCN, Mg(CN)2 |
CN |
cyanure |
I |
| HNO2, Ba(NO2)2 |
NO2 |
nitrite |
I |
| HNO3, Al(NO3)3 |
NO3 |
nitrate |
I |
| NaClO, KClO |
ClO |
hypochlorite |
I |
| KClO2, Mg(ClO2)2 |
ClO2 |
chlorite |
I |
| NaClO3, Zn(ClO3)2 |
ClO3 |
chlorate |
I |
| HClO4, KClO4 |
ClO4 |
perchlorate |
I |
| Na2CO3, FeCO3 |
CO3 |
carbonate |
II |
| H2SO3, CaSO3 |
SO3 |
sulfite |
II |
| K2SO4, Al2(SO4)3 |
SO4 |
sulfate |
II |
| H3PO3 |
PO3 |
phosphite |
III |
| H3PO4, Be3(PO4)2 |
PO4 |
phosphate |
III |
| NaHCO3, KHCO3 |
HCO3 |
bicarbonate |
I |
| KMnO4 |
MnO4 |
permanganate |
I |
INTRODUCTION | OBSERVATION | DEFINITION | VALENCE DES
ATOMES | VALENCE DES
RADICAUX
| RADICAL
ET MOLECULE
| EXERCICES 1 | EXERCICES 2 | MOTS
CROISES
 Un radical
n'est pas une molécule Un radical
n'est pas une molécule 
Comment expliquer la
valence d'un radical?
exemple: le radical
hydroxyle (ou hydroxyde) a la valence I
- on sait que
l'atome d'oxygène O a la valence II:
 il possède 2 bras de valence il possède 2 bras de valence
- on sait que
l'atome d'hydrogène H a la valence I:
 il possède 1 bras de valence
il possède 1 bras de valence
- donc le radical
OH a la valence I:
 il possède 1 bras de valence libre il possède 1 bras de valence libre
| Un radical est un groupement d'atomes
associés; ce groupement d'atomes a une valence et peut donc s'associer à
d'autres atomes ou d'autres radicaux pour former une
molécule. |
| Une molécule est un groupement d'atomes
associés dont les bras de valence sont tous occupés,
une molécule a donc une valence
nulle. |
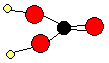
exemple
de molécule (donc valence nulle): NaOH 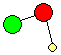 (hydroxyde de sodium) (hydroxyde de sodium)
INTRODUCTION | OBSERVATION | DEFINITION | VALENCE DES
ATOMES | VALENCE DES
RADICAUX
| RADICAL
ET MOLECULE
| EXERCICES 1 | EXERCICES 2 | MOTS
CROISES
 Exercices du premier type: recherche de la formule d'un
corps pur composé Exercices du premier type: recherche de la formule d'un
corps pur composé
| quelle
est la formule du corps pur dont la
molécule contient de l'aluminium et de l'oxygène? |
quelle
est la formule du corps pur dont la
molécule contient du silicium et de l'oxygène? |
| Al
(III), O (II) |
Si
(IV), O (II) |
| réponse: Al2O3 |
réponse: SiO2
et pas Si2O4 |
 Procédé du chiasme: on croise les valences et
on obtient les indices; veiller à ce que les indices
soient premiers entre eux, sinon il faut les diviser par
leur PGCD.
Procédé du chiasme: on croise les valences et
on obtient les indices; veiller à ce que les indices
soient premiers entre eux, sinon il faut les diviser par
leur PGCD. Procédé de la structure qui permet une meilleure
compréhension par la visualisation
Procédé de la structure qui permet une meilleure
compréhension par la visualisation
(ci-dessous)
|
| structure
de la molécule: 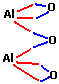
|
structure
de la molécule: 
|
| quelle
est la formule du corps pur dont la
molécule contient du sodium et du sulfate? |
quelle
est la formule du corps pur dont la
molécule contient de l'ammonium et du soufre? |
| Na
(I), SO4
(II) |
NH4
(I), S(II) |
| réponse: Na2SO4 |
réponse: (NH4)2S |
| structure
de la molécule: 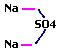
|
structure
de la molécule: 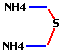
|
 Exercices du second type: recherche de la valence d'un
atome ou radical Exercices du second type: recherche de la valence d'un
atome ou radical
| quelle
est la valence du phosphore dans PCl3? |
quelle
est la valence de l'azote dans N2O3? |
| on
sait que le chlore Cl a toujours la valence I, mais le phosphose se
comporte parfois comme s'il avait une autre valence que
celle indiquée par le tableau périodique (III) |
on
sait que l'oxygène O a toujours la valence II, mais l'azote se comporte
parfois comme s'il avait une autre valence que celle
indiquée par le tableau périodique (III) |
| structure
de la molécule: 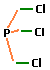
|
structure
de la molécule: 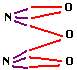
|
| réponse: le phosphore P a la
valence III dans PCl3 |
réponse: l'azote N a la valence III dans N2O3 |
| quelle
est la valence du plomb dans PbO2? |
quelle
est la valence du radical phosphate dans
Ca3(PO4)2? |
| on
sait que l'oxygène O a toujours la valence II, mais le plomb Pb peut
avoir la valence II ou IV |
on
sait que le calcium Ca a toujours la valence II, mais vous avez oublié la
valence du radical phosphate |
| structure
de la molécule: 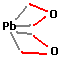
|
structure
de la molécule: 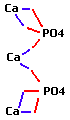
|
| réponse: le plomb a la valence IV dans PbO2 |
réponse: le radical phosphate a la
valence III dans Ca3(PO4)2 |
INTRODUCTION | OBSERVATION | DEFINITION | VALENCE DES
ATOMES | VALENCE DES
RADICAUX
| RADICAL
ET MOLECULE
| EXERCICES 1 | EXERCICES 2 | MOTS
CROISES
RETOUR
|





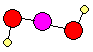
 (hydroxyde de sodium)
(hydroxyde de sodium)